Evidence
効果効能
-
健康食品/飲む
-
化粧品/塗る
安全性評価に関する調査研究
研究課題既存天然添加物の安全性評価に関する調査研究
- 共同研究者
- 厚生省生活衛生局食品化学課監修
日本食品添加物協会
アウレオバシジウム培養液
1.食品添加物名
アウレオバシジウム培養液 (Aureobasidium cultured solution)
2.起原・製法・本質
黒酵母(Aureobasidium Pullulans)の培養液より、分離して得られたものである。
主成分はβ-1,3-1,6-グルカンである。
3.主な用途
増粘安定剤
4.安全性試験成績の慨要
-
単回投与試験
1 急性経口 LD 50はラットで 6,000mg/kg 超、マウスで 7,500mg/kg 超である。 -
反復投与試験
SD ラットを用いた強制経口(300.600.1,200.2,400mg/kg)投与による 3 ヶ月間の反腹投与試験において、検体投与に起因する毒性学的影響は認められていない。無毒性量は 2,400mg/kg/day と考えられる。 -
変異原性試験
細菌を用いた復帰変異試験、哺乳類培養細胞を用いた染色体異常試験の結果は、いずれも陰性と判断される。 -
眼粘膜刺激性試験
日本白色ウサギを用いて眼の角膜、結膜及び虹彩に対する一次刺激性を 3.0%水溶液で調べた試験の結果は、陰性と認められている。
引用文献
- 今井 清ほか:MST(ムタステイン)の経口投与によるラットにおける急性毒性試験、基礎と臨床,20(12),131,Sep.1986
- 今井 清ほか:MST(ムタステイン)の経口投与によるマウスにおける急性毒性試験,基礎と臨床,20(12),133,Sep.1986
- 山口 一喜ほか:MST(ムタステイン)のラットにおける経口 3 ヶ月間投与における毒性試験,基礎と臨床,20(12),135 Sep.1986
- 田中 憲穂ほか:MST(ムタステイン)のチャイニーズハムスター培養細胞による染色体試験、基礎と臨床,20(12),127,Sep,1986
- 岩原 繁雄ほか:MST(ムタステイン)の細菌による変異原性試験報告,基礎と臨床, 20(12), 123, Sep,1986
- 原 康夫ほか:ムタステインの眼粘膜刺激性試験,基礎と臨床, 23(2),71,Jan,1989
アレルギーに対する効果
研究課題アウレオバシジウム属菌株培養液(ACFA gMax)のI型アレルギー反応抑制に関する効果について
( 皮膚炎発症モデルマウスNC/Ngaを用いた動物実験による検討)
目的
I型アレルギー反応の検定には、通常の肉眼的皮膚所見をもとに、血中の総 IgE 量の測定、抗原特異的IgE 量の測定、血中および皮膚病変部浸潤好酸球数測定、ヒスタミン放出(遊離)量の測定、Th1/Th2 の免疫系バランスをサイトカイン(IL-4、IEN-r、etc)産生量等による推察、さらには CD4/CD8 リンパ球の解析等さまざまな検討が必要とされている。
今回、我々は黒酵母の一種であるアウレオバシジウム属菌株培養液のI型アレルギー反応抑制に対する相対的な基本的データを得ることを目的とし、皮膚炎発症モデルマウス(アトピー性皮膚炎自然発症マウス、NC/Nga mouse)を用いた動物実験により、肉眼的病理所見ならびに血中 IgE 総量の経時的測定を行い、アウレオバシジウム属菌株培養液投与、非投与群間における有効性の差異を検索することで、同成分の抗アレルギー作用(効果)の有用性について検討した。
実験用試験試料
アウレオバシジウム属菌株培養液 商品名:ACFAgMax (一光化学株式会社製造)
実験動物ならびに実験方法
1.被験試料の作成
上記実験用被験試料をヒト(平均体重 60Kg)の平均の摂取量(40ml)より換算した値を、ヒトおよびマウス(約 20g)の体重比より算出し、さらにこの量の約 25~30 倍摂取濃度(経口投与実験設定濃度)となる様に設定した量を計算し、通常のマウス飼育用粉餌の中へ均等に混合した後、飼料の固形型打ち、ならびに放射線滅菌した物を作成し、被験飼料として用いた。(マウス飼料中の実質濃度=約 5%濃度)
なお、control 群は通常のマウス滅菌固形飼料のみの摂取により実施した。
2.実験動物
NC/Nga mouse, clean, CV(生後 4 週齢を日本 SLC(株)より入手)を用い、雄雌それぞれ 1 群 10 匹の系で行い、上記の被験試料投与群および control 群の、計 4 群にて行った。
上記実験動物はすべて入荷後 1 週間の予備飼育の後、第 5 週齢より第 16 週齢に至るまでの間を観察期間とした。
飼育条件は室温 24±1°C、相対湿度 55±5%、明暗各 12 時間(照明時間:午前 7 時~午後 7 時)、ヘパフィルターにより除菌された新鮮空気による換気回数:12 回以上/時に設定されたバリアシステム動物飼育室(マウス、ラット室)で飼育した。 飼育には滅菌床敷(ホワイトフレーク、日本チャールズリバー社)を入れた、滅菌済みのプラスチック製ケージ(47×31×20 cm)を用いて 4~6 匹飼いで飼育した。 飼育ケージの交換は週 1 回行った。また、飼料は固形飼料(CRF-1、オリエンタル酵母社)を給餌器(ケージトップ)に入れ、飲料水は水道水を滅菌給水瓶に入れてそれぞれ自由に摂取させ飼育した。
3.実験方法
血中 IgE 量の測定については、試料摂取の1週後(6 週齢)、4週後(9 週齢)、7 週後(12 週齢)、11 週後(16 週齢)の 4 回に渡り、マウス眼底静脈層より採血を行い、得られた血清中の IgE 総量の経時的変化をマウス IgE に対する特異抗体を用いたサンドウィッチエライザ法(酵素抗体法)により算出した。
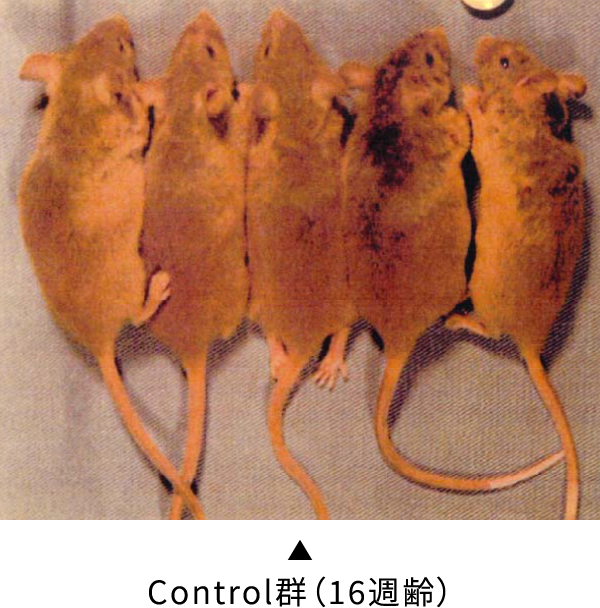
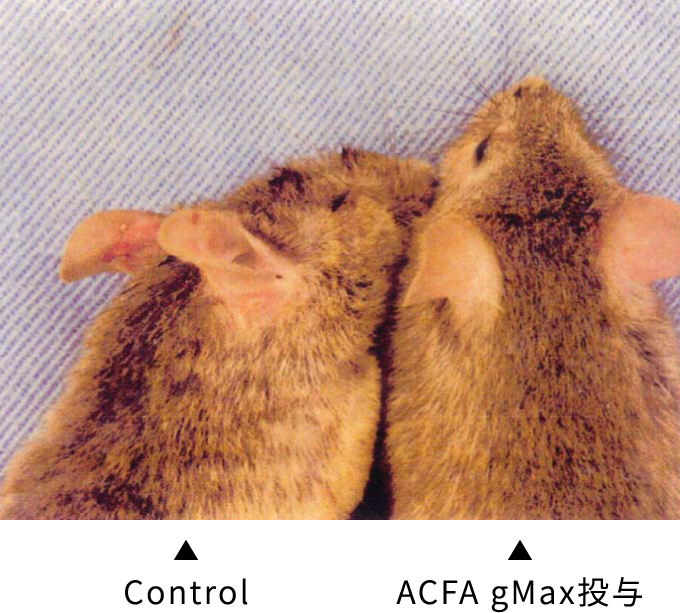
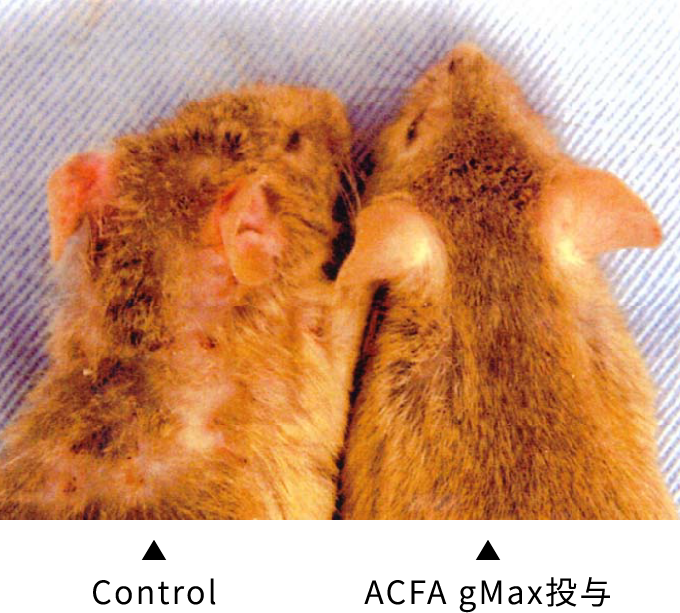
また、投与 11 週後(16 週齢)における肉眼的皮膚所見について観察比較した。
実験結果
上記被験試料の混合飼料摂取群においては、control 群と比較し有意に血中 IgE 産生の抑制が認められる結果が得られた。
特に、投与 11 週後(16 週齢)における血中 IgE 値では、雄雌の両群において統計学的に t 検定を行ったところ、危険率 p<0.05 上での有意な差異が認められた。
また、16 週齢(通常のアレルギー自然発症週齢)における肉眼的皮膚所見においては、contro1 群と比較し、被験試料混合飼料摂取群において明らかに皮膚アレルギー症状の抑制傾向が認められた。
総括
今回我々は、皮膚炎発症モデルマウス NC/Nga を用いた動物実験によるI型アレルギー反応抑制に関する効果について、血中 IgE 総量を経時的に測定することで検討を行った。検討試料としては、アウレオバシジウム属菌株培養液 商品名:ACFA gMax(一光化学株式会社製)を用いて行い、生後第5週より第 16週までの間において被験試料を自由摂取させることで血中 IgE 産生の変動を観察した。
その結果、control 群を含むすべての NC/Nga マウス群において血中 IgE 総量は、個体の発育とともに上昇傾向が認められたが、上記被験試料投与群においては control 群に比べ明らかにその産生抑制効果が確認された。同様に、皮膚アレルギー症状の抑制作用についても被験試料投与群においては control 群に比べその発症抑制効果が確認された。
以上の結果より、アウレオバシジウム属菌株培養液 商品名:ACFA gMax のI型アレルギー反応の発症抑制に関する効果が動物実験により明らかにされ、同等成分の人摂取におけるアレルギー反応発生抑制に有効であることが示唆された。
| NC/Nga mouse(♂)血中IgE値の加齢による変動 | ||
|---|---|---|
| Week(週齢) | Control群(μg/ml) | ACFAgMax投与群(μg/ml) |
| 6 | 7.5±2.97 | 8.3±4.9 |
| 9 | 26.8±5.9 | 24.3±3.4 |
| 12 | 90.2±15.9 | 74.4±10.7 |
| 16 | 160.1±39.9(p<0.05) (mean±SD,n=10) |
103.1±23.4(p<0.05) (mean±SD,n=10) |
 |
||
| NC/Nga mouse(♀)血中IgE値の加齢による変動 | ||
|---|---|---|
| Week(週齢) | Control群(μg/ml) | ACFAgMax投与群(μg/ml) |
| 6 | 6.3±2.2 | 8.2±3.8 |
| 9 | 25.8±6.3 | 22±4.7 |
| 12 | 85.9±16.6 | 73±9.4 |
| 16 | 170.3±74.5(p<0.05) (mean±SD,n=10) |
97.3±21.8(p<0.05) (mean±SD,n=10) |
 |
||

がんに対する効果
研究課題アクファジーマックス腫瘍抑制比較実験:抗腫瘍活性
実験方法
細胞の調整:下記 6 種類の腫瘍細胞を各細胞株とも 37°C/5%CO2 インキュベータ中で、10%FCS を含む RPMl1640 培養液環境下、25㎠培養フラスク内で浮遊増殖培養を行い、対数増殖期にある時点でRPMl1640 培養液環境下に洗浄置換して細胞数が 400000~8000000cells/ml となるように調整した。
〔腫瘍細胞〕
- CCRF-CEM 細胞:T 細胞系のリンパ系白血病由来のヒト腫瘍細胞
- K562 細胞:T 細胞系のリンパ系白血病由来のヒト腫瘍細胞
- MOLT-4CL#8 細胞:T 細胞系のリンパ系白血病由来のヒト腫瘍細胞
- U937 細胞:マクロファージ系のリンパ系白血病由来のヒト腫瘍細胞
- Raji 細胞:B 細胞系のリンパ系白血病由来のヒト腫瘍細胞
- YAC-1 細胞:ナチュラルキラー細胞に感受性を持つマウスのリンパ腫細胞
アクファおよび Agaricus Blazei 由来抽出成分等の調製法
- アクファ(アクファジーマックス):黒酵母発酵液+リンゴ抽出物を超音波破砕機(ultrasonicDisruptor UR-200P)を用い、200W/20 min. sonication 処理後、超遠心操作(35,000 rpm,30 min.)により上清を得、これを出発材料として 10 倍希釈溶液(原液の 1%溶液)、20 倍、100 倍希釈溶液となるように Na-Phosphate Bufferd Saline(PBS)で希釈したものを作成し、これを 0.22μmフィルターにて無菌ろ過し、被験材料とした。
- マイセリアゴールド:マイセリアゴールド菌糸体培養上清(濾液を含む)乾燥粉末を 10%(w/v 濃度となるようイオン交換水に懸濁し、超音波破砕機(Ultrasonic Disruptor UR-200P)を用い、200 W/ 10 min. sonication 処理後、同混液を 2hr.熱水抽出操作を行った。その後、超遠心操作(35,000rpm/30 min.)により上清を得、これを出発材料重量より換算して final 1%濃度となるように HEPESGood bulffer(pH 7.4,μ0.15)にて希釈し、被験材料とした。
- 菌糸体:マイセリア菌糸体培養上清(約 10L 培養液の 200 メッシュ上清)凍結品を解凍後、イオン交換水で十分に洗浄後、HEPES Goad buffer(pH 7.4,μ0.15)に懸濁した。さらに 1.と同様にsonication 処理、熱水抽出操作、超遠心操作を行い抽出成分(350mL の菌糸体由来成分)を得、これを 10 倍希釈したものを被験材料とした。
- 子実体:マイセリア子実体乾燥粉末を 10%(w/v)濃度となるよう HEPES Good buffer(pH.7.4,μ0.15)に懸濁し、さらに 1.と同様に sonication 処理、熱水抽出操作、超遠心操作を行い抽出成分を得た。
また 1.と同様に重量より換算して final 1%濃度となるように希釈し、被験材料とした。 - ビール酵母:マイセリアゴールド菌糸体培養上清(濾液を含む)乾燥粉末と同様の組成となるように、ビール酵母、ラクトース、デキストリンにより調製し、菌糸体のみを含まないものを作成した。抽出操作等は 1.と同様に行い、被験材料とした。
さらに、1.~6.の調整培養細胞浮遊液をそれぞれ 96well cell culture 中に 100μL ずつ分注し、この中に各被験材料を等量添加し、よく混合した後、再び 37°C/5%CO2 インキュベーター中で 36 時間反応培養を行った。
これらの各培養細胞を 0.5%Trypan blue にて染色し、反応後の生細胞の数を計測し、Control(PBS)と比較することで各腫瘍細胞に対する抗腫瘍(増殖抑制)活性として算出した。
結果
ACFA(アクファ)成分の血液腫瘍細胞に対する抗腫瘍(増殖抑制)活性
| 腫瘍細胞 | 10倍 | Cont | 抑制率 | 20倍 | Cont | 抑制率 | 100倍 | Cont | 抑制率 |
|---|---|---|---|---|---|---|---|---|---|
| 生細胞数 | 生細胞数 | % | 生細胞数 | 生細胞数 | % | 生細胞数 | 生細胞数 | % | |
| CCRF-CEM CELL (急性リンパ性白血病) |
499 | 2038 | 75% | 874 | 1934 | 55% | 1477 | 1997 | 26% |
| K562 CELL (慢性骨髄炎) |
250 | 2350 | 89% | 1290 | 2444 | 47% | 1643 | 2371 | 31% |
| MOLT-4CL#8 CEL (急性リンパ性白血病) |
260 | 1997 | 87% | 499 | 2028 | 75% | 1508 | 1955 | 23% |
| U937 CELL (組織リンパ腫) |
52 | 1716 | 97% | 1165 | 1716 | 32% | 1716 | 1747 | 2% |
| Raji cell (バーキットリンパ腫) |
0 | 1976 | 100% | 603 | 1893 | 68% | 874 | 1924 | 55% |
| YAC-1 CELL (マウス、リンパ腫) |
218 | 1820 | 88% | 499 | 1893 | 74% | 1092 | 2018 | 46% |
Agaricus Blazei 由来抽出成分の血液腫瘍細胞に対する抗腫瘍(増殖抑制)効果 比較
- CCRF-CEM CELL(急性リンパ性白血病)
- K562 CELL(慢性骨髄炎)
- MOLT-4CL#8 CEL(急性リンパ性白血病)
- U937 CELL(組織リンパ腫)
- Raji cell(バーキットリンパ腫)
- YAC-1 CELL(マウス、NK 細胞感受性リンパ腫)
| 希釈濃度 | ×10 | ×20 | ×100 | |||
|---|---|---|---|---|---|---|
| 検体 | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) |
| Control (HPESbuffer) |
19.6 | 100 | 18.6 | 100 | 19.2 | 100 |
| アクファ | 4.8 | 24.5 | 8.4 | 45.2 | 14.2 | 74.0 |
| マイセリアゴールド | 4.2 | 21.4 | 8.8 | 47.3 | 15.5 | 80.7 |
| 菌糸体 | 6.5 | 33.2 | 10.4 | 56.0 | 15.8 | 82.3 |
| 子実体 | 3.5 | 17.9 | 7.5 | 40.3 | 12.8 | 66.7 |
| ビール酵母 | 13.4 | 68.4 | 16.8 | 90.3 | 17.5 | 91.1 |
アクファには明らかに血液腫瘍細胞の増殖抑制効果が認められた。
| 希釈濃度 | ×10 | ×20 | ×100 | |||
|---|---|---|---|---|---|---|
| 検体 | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) |
| Control (HPESbuffer) |
22.6 | 100 | 23.5 | 100 | 22.8 | 100 |
| アクファ | 2.4 | 10.6 | 12.4 | 52.8 | 15.8 | 69.3 |
| マイセリアゴールド | 1.1 | 4.9 | 4.2 | 17.9 | 14.5 | 63.6 |
| 菌糸体 | 2.6 | 11.5 | 8.4 | 35.7 | 16.8 | 73.7 |
| 子実体 | 0.8 | 3.5 | 10.2 | 43.4 | 16.2 | 71.1 |
| ビール酵母 | 17.8 | 78.8 | 20.5 | 87.2 | 21.4 | 93.9 |
アクファには明らかに血液腫瘍細胞の増殖抑制効果が認められた。
| 希釈濃度 | ×10 | ×20 | ×100 | |||
|---|---|---|---|---|---|---|
| 検体 | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) |
| Control (HPESbuffer) |
19.2 | 100 | 19.5 | 100 | 18.8 | 100 |
| アクファ | 2.5 | 13.0 | 4.8 | 24.6 | 14.5 | 77.1 |
| マイセリアゴールド | 1.8 | 9.4 | 5.6 | 28.7 | 8.8 | 46.8 |
| 菌糸体 | 3.6 | 18.5 | 12.4 | 63.6 | 17.5 | 93.1 |
| 子実体 | 2.2 | 11.5 | 4.6 | 23.6 | 15.8 | 84.0 |
| ビール酵母 | 10.8 | 56.3 | 14.5 | 73.3 | 17.9 | 95.2 |
アクファには明らかに血液腫瘍細胞の増殖抑制効果が認められた。
| 希釈濃度 | ×10 | ×20 | ×100 | |||
|---|---|---|---|---|---|---|
| 検体 | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) |
| Control (HPESbuffer) |
16.5 | 100 | 16.5 | 100 | 16.8 | 100 |
| アクファ | 0.5 | 3.0 | 11.2 | 67.9 | 16.5 | 98.2 |
| マイセリアゴールド | 0.6 | 3.6 | 12.0 | 72.7 | 16.5 | 98.2 |
| 菌糸体 | 14.0 | 84.8 | 11.0 | 66.7 | 17.8 | 106.0 |
| 子実体 | 1.2 | 7.3 | 10.0 | 60.6 | 14.5 | 86.3 |
| ビール酵母 | 10.5 | 63.6 | 12.2 | 74.0 | 15.5 | 92.3 |
アクファには明らかに血液腫瘍細胞の増殖抑制効果が認められた。
| 希釈濃度 | ×10 | ×20 | ×100 | |||
|---|---|---|---|---|---|---|
| 検体 | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) |
| Control (HPESbuffer) |
19.0 | 100 | 18.2 | 100 | 18.5 | 100 |
| アクファ | 0 | 0 | 5.8 | 31.9 | 8.4 | 45.4 |
| マイセリアゴールド | 0 | 0 | 6.2 | 34.1 | 8.8 | 47.6 |
| 菌糸体 | 0.5 | 2.6 | 8.0 | 44.0 | 8.8 | 47.6 |
| 子実体 | 0.5 | 2.6 | 0 | 18.2 | 4.5 | 24.3 |
| ビール酵母 | 5.5 | 28.4 | 18.5 | 102 | 18.5 | 100 |
アクファには明らかに血液腫瘍細胞の増殖抑制効果が認められた。
| 希釈濃度 | ×10 | ×20 | ×100 | |||
|---|---|---|---|---|---|---|
| 検体 | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) | 生細胞数(1×104) | 生/死細胞比(%) |
| Control (HPESbuffer) |
17.5 | 100 | 18.2 | 100 | 19.4 | 100 |
| アクファ | 2.1 | 12.0 | 4.8 | 26.4 | 10.5 | 54.1 |
| マイセリアゴールド | 1.5 | 8.6 | 4.5 | 24.7 | 7.8 | 40.2 |
| 菌糸体 | 1.5 | 84.8 | 8.8 | 48.4 | 13.8 | 71.1 |
| 子実体 | 1.8 | 10.3 | 2.2 | 12.1 | 8.5 | 43.8 |
| ビール酵母 | 10.4 | 59.4 | 14.5 | 79.7 | 17.5 | 90.2 |
アクファには明らかに血液腫瘍細胞の増殖抑制効果が認められた。
研究課題アクファジーマックス腫瘍抑制比較実験:腫瘍抑制率
実験方法
Sarcoma 180 固型癌の移植:Sarcoma 180 細胞株を 37 ℃ X/5%CO2 インキュベータ中、10%FCS/RPMI l640 培養液にて継代培養した。対数増殖期(Full seat)にある同細胞を Trypsin-EDTA により培養フラスクより剥離した後、PRMI‐1640 培養液で洗浄し、細胞数を 5×10 cells /mLとなるように調製したものを使用した。動物への投与は、この 0.1mL をそれぞれの被験マウス背部皮下に移植した。なお、操作はすべて無菌的に行った。
アクファ(アクファジーマックス)成分の調整法
アクファを超音波破砕機(Ultrasonic Disruptor UR-200P)を用い、200W/20min.sonication 処理後、超遠心操作(35000rpm/30min.)により上清を得、これを HEPES Good buffer(ph7.4,μ0.15)にて 10 倍希釈したものを被験材料とした。
抽出成分の投与量および方法
マウスに Sarcoma180 固形癌細胞移植 24 時間後より、アクファ被験材料を、0.22μm フィルターにて無菌ろ過したものを、1 日 1 回(0.1ml)すつ、それぞれ 14 日間、腹腔内(ip)投与した。
結果
| 投与群 | 腫瘍重量(g) | 腫瘍抑制率(%) | |||||
|---|---|---|---|---|---|---|---|
| No.1 | No.2 | No.3 | No.4 | No.5 | Mean | ||
| Control(PBS) | 2.64 | 3.82 | 3.57 | 1.89 | 2.24 | 2.83 | 0 |
| ACFA(アクファ) | 0.39 | 1.11 | 0.18 | 0.28 | 0.58 | 0.51 | 82 |
アクファには明らかに腫瘍抑制効果が認められた。
放射能に対する効果
研究課題アクファの特徴について
目的
医学、薬学、栄養学、医療診断機器等の進歩により、我国は世界で最も平均寿命の長い国に成っている。このような長寿命化が更に進むと、様々な生活習慣病が発生する。この様な疾患に対して健康維持への関心が高まっている。
このような観点からアクファ(アクファジーマックス)は天然物であり、アクファに含まれる様々な成分(多糖類)によって、健康が維持できるならば老人にとって朗報となる。
また、自然被爆による健康への影響も問題化している。その代表的なものに航空機に乗務する操縦士やキャビンアテンダントであり、地上から 1 万mの超高空になると宇宙線による被爆が加わって、被爆は一般人の 2 倍以上となり、健康への影響も無視出来ない。また、原子力施設に勤務する人々にとっても自然被爆の他に放射線源からの微量被爆やイラク・イラク等へ派遣される自衛隊員の劣化ウラン弾による被爆等色々な被爆が考えられる。アクファにはこれらの放射線損傷に対する防護効果があり、更に免疫効果を増強させる作用もあるため、被爆後の健康維持に役立つと考えられる。
試験内容と結果
アクファの毒性試験
アクファを 0.3cc/1 回/日/匹から 3cc/3 回/日/匹で、C3H マウス(♂、6 週令)に毎日 15 日間ゾンデによる経口投与を行った。
その結果、投与期間内にはマウスの死亡は観測されなかった。投与終了後、更に 20 日間の生存観測を行ったが、観測期間内にはマウスの死亡は見られなかった。この事から半致死量は5cc/日/匹以上と推測される。この量は 60kg の人体に換算すると、12 リットルの量を 15 日間毎日摂取した事になり、アクファには毒性は全く無いと言える。
アクファの血球への影響
アクファによる血球への影響として以下の7項目について調べた。
-
RBC(赤血球数;104/μL):酸素の運搬、炭酸ガス運搬
アクファは赤血球には変化を及ぼさない。 -
WBC(白血球;/μL):免疫能に関与、感染に関与
アクファ投与後 2 日間の間、白血球は 1.5 から 2.0 倍の増加が観測された。その作用は投与後、約 2 日間程度持続し、免疫能活性が出現した。 -
MO(単球;%):貧食・殺菌機能、炎症・免疫に関与
アクファ投与後2日間に単球は3倍の上昇が観測され、抗炎症効果、免疫能活性効果が出現した。 -
LY(リンパ球;%):白血球の一種で免疫に関与
アクファ投与により、リンパ球数の増加は認めないが、リンパ球自体の活性度が増加した。 -
HGB(血色素;g/dL):酸素運搬機能、炭酸ガス運搬機能
アクファ投与は血色素へは影響しない。 -
HCT(ヘマトクリット;%):赤血球容積率
アクファ投与によるヘマトクリットへの影響はない。 -
MCV(平均赤血球容積;fL):赤血球 1 個当りの平均体積
アクファ投与による平均赤血球容積への影響はない。
アクファの抗酸化作用
アクファには強い抗酸化作用が見られ、抗酸化作用は組織内の酸素を除去するために、放射線に対して組織は抵抗性となる。組織内の酸素が減少すると放射線の効果が減少する事が判っており、抗酸化物質が体内に摂取されると組織内酸素分圧は減少するので放射線に対して抵抗性となる。従って、アクファの摂取は組織内を低酸素にする可能性があり、放射線防護作用が出現する。
アクファの放射線防護効果
アクファ投与後のマウスに放射線を1回全身照射し、腸管への放射線障害を調べると、アクファ非投与群より、腸管は放射線損傷がなく、アクファによる放射線防護効果が確認された。
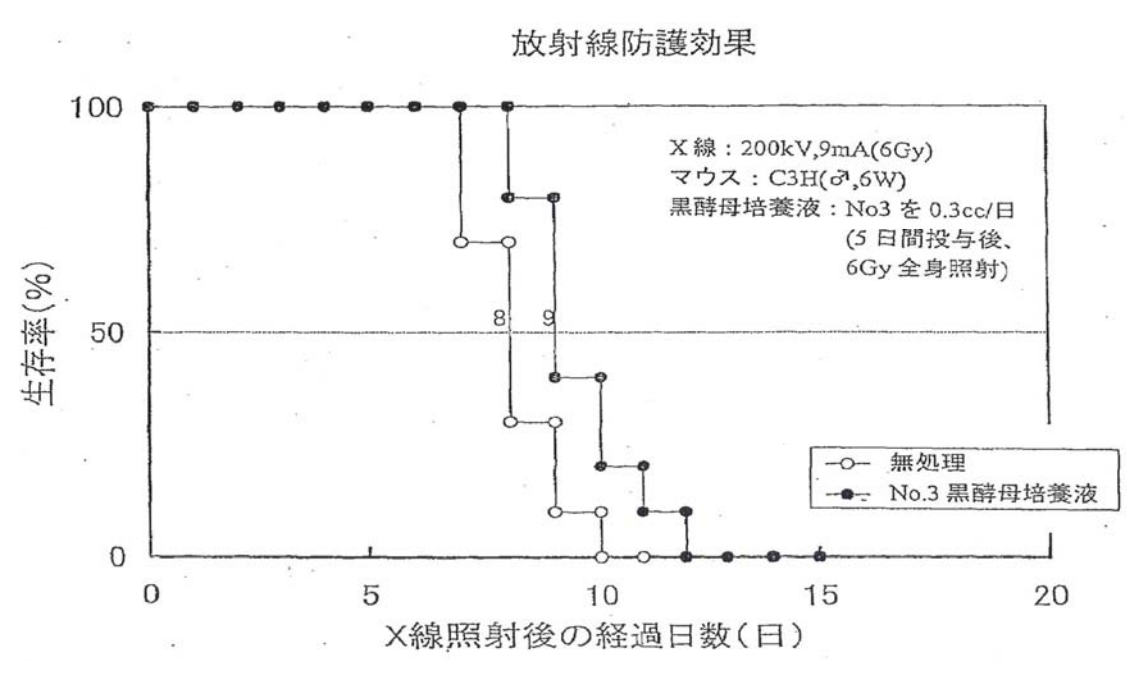
アクファの抗腫瘍効果
担癌マウスにアクファを連日投与すると、マウス白血球の活性化に伴って、腫瘍が免疫細胞により攻撃され、腫瘍組織は破壊され、アクファによる腫瘍縮小を示した。
この事は発癌を抑制し、癌治療後の患者の予後を良好にする可能性が高い事を示している。
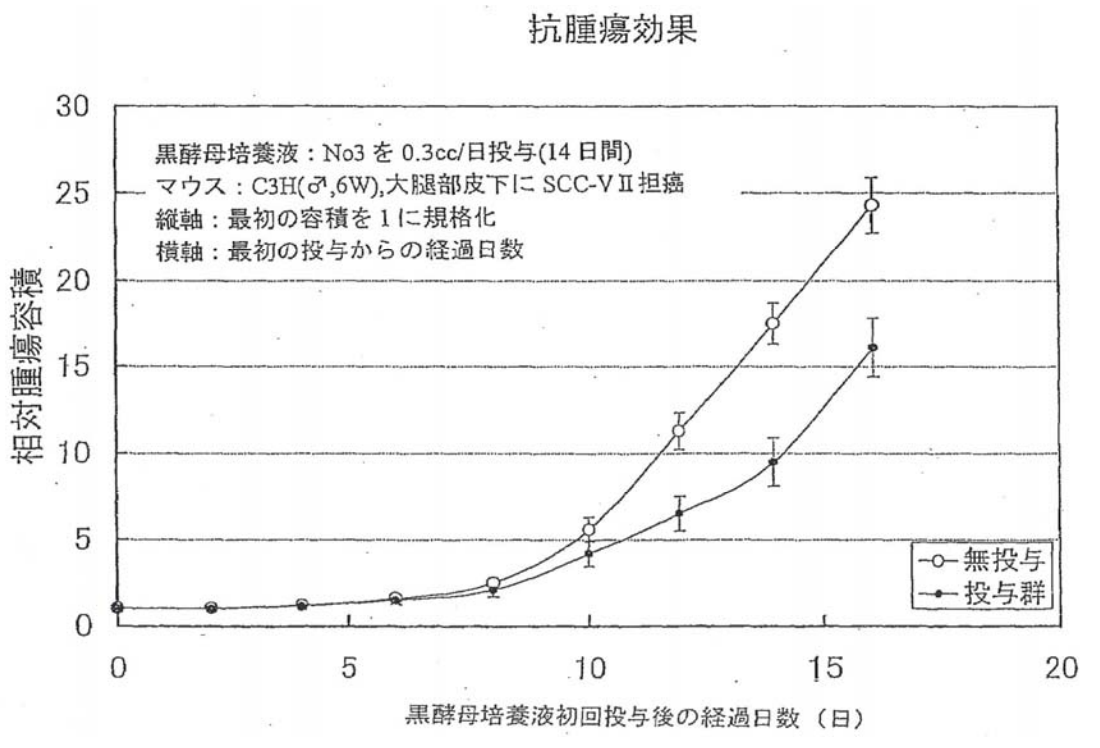
アクファによる体重変化
アクファ投与後 15 日頃から無投与群よりもアクファ投与群は有意に体重増加が見られ、アクファによる栄養吸収能増加またはアクファの栄養成分による体重増加が確認された。
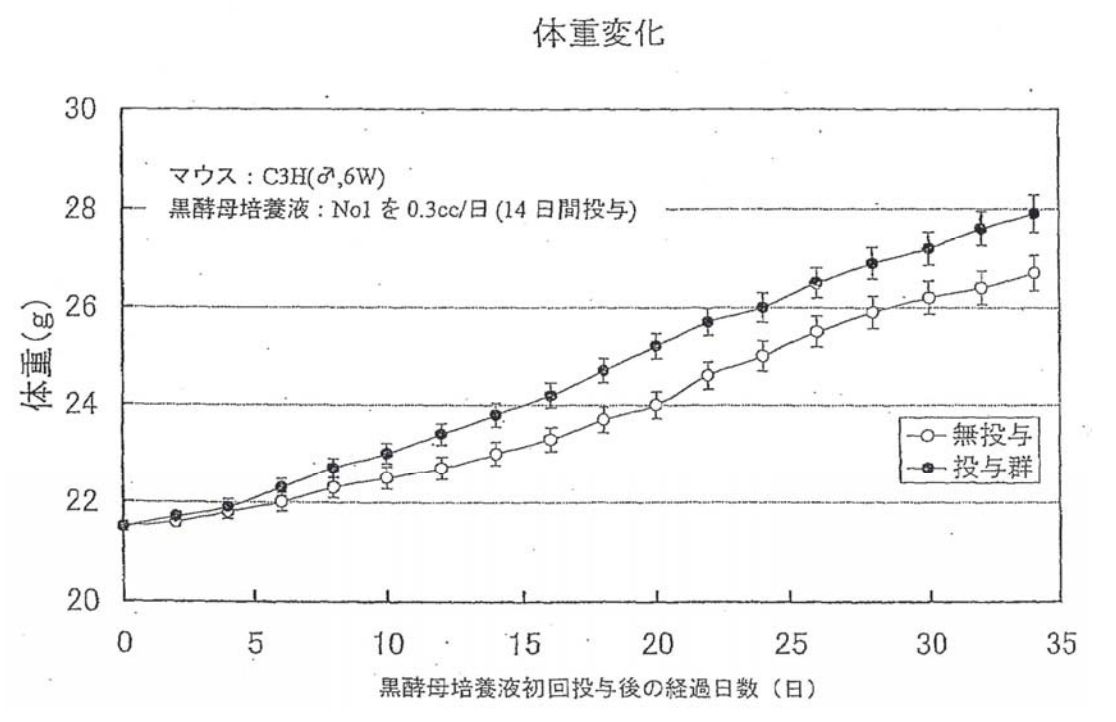
考察・総括
考察
- アクファには毒性がない。
- アクファには白血球増加効果がある。
- アクファにはリンパ球へ活性効果がある。
- アクファには平均赤血球容積への影響は無い。
- アクファには抗腫瘍効果がある。
- アクファには体重減少抑制作用がある。
- アクファには赤血球への影響は無い。
- アクファには単球増加効果がある。
- アクファには血色素への影響は無い。
- アクファには抗酸化作用がある。
- アクファには放射線防護作用がある。
以上の結果からアクファには消炎症効果、免疫能活性化、抗腫瘍効果、放射線障害予防効果等のある事がわかる。
総括
- 黒酵母グルカンには免疫能活性作用があり、そのために体力低下による感染や疾患発病に対して抑制効果が期待できる。
- 黒酵母グルカンには微弱から中程度(4Gy 全身被爆)の放射線被爆に対して、放射線障害防護作用があり、ウラン弾による被爆に射して血液障害、骨髄障害、腸管障害等の放射線障害の防護作用が期待できる。
- 黒酵母グルカンには制癌効果があり、さらに免疫能低下による発癌を抑制する作用があり、体力消耗に伴った発癌を抑制する効果がある。更にウラン弾やその他の放射線による被爆に伴う発癌への抑制も期待できる。
- 黒酵母グルカンに体重減少抑制効果があり、体力消耗時の体重減少を抑制するため、重労働時の体調を正常に維持することが期待できる。
以上の結果は実験動物(C3H/Hej マウス)によって実証されており、哺乳類(人類)に対して同様な効果が期待できる。
服用に際しては一度に多量を摂取せずに、1 日に 4 から 6 回に分けて摂取する方が効率良く作用する。
ヒト皮膚への刺激性評価
研究課題アウレオバシジウム M‐P04 のヒト皮膚刺激性試験
- 試験実施責任者
- 株式会社河合産業皮膚医学研究所 医師 河合 敬一
試験の目的
アウレオバシジウム M‐P04 の皮膚刺激性を評価するため、アウレオバシジウム M-P04 のヒト皮膚刺激性試験を実施した。
対象および試験品
対象
健常成人 40 名を対象とし、あらかじめ被験者に試験の主旨を説明し、被験者の同意を得た後に試験を行った。被験者 40 名(男性 14 名、女性 26 名)の年齢は 28 歳~57 歳で、平均年齢は 45.9 歳であった。なお、本試験に参加した被験者はヒトパッチテストに好ましい下記の諸条件1)~5)を満たした。
- 年齢が 18 歳以上
- 妊娠していない
- 授乳中でない
- 試験試料に過敏症の既往歴がない
- 皮膚疾患の現症がない
- 片方の性が3分の1以上ある
- 試験1週間前から試験終了まで、ステロイド剤等のパッチテスト反応を軽減する可能性の高い薬剤の注射・内服・被験部への外用がない
- 試験期間中に過激な運動をせず、過剰な汗をかかない
- 試験2週間前から試験終了まで、被験部を日焼けさせない
試験品
- アウレオバシジウム M‐P04(原液)
- 精製水(原液、(1)の対照試料) 試験前に各試験品に配合されている各成分の配合濃度、構造活性および物理化学特性を検討し、重篤な皮膚障害を起こす可能性が低いと判断し、試験を実施した。
アウレオバシジウムM-P04の成分表
| 成分名 | 配合比率(%) |
|---|---|
| アウレオバシジウムプルランス培養液 | 99.80 |
| メチルパラベン | 0.15 |
| エチルパラベン | 0.05 |
試験期間中の外的環境
試験期間(2005 年 2 月 15 日~17 日)の京都市の気象状況を第 2 表に示した。
試験方法
フィンチャンバー© (8 mmφ, EPITEST Ltd, フィンランド)およびスカンポールテープ©(AlpharmaA/Sノルウェー)を用い、上記試験品(15μl)を上背部皮膚に 24 時間閉塞貼付した。
判定方法
試料除去 1 時間後および 24 時間後の皮膚反応を本邦基準6)(第3表)に従って肉眼判定した。
本邦基準判定
| 皮膚反応 | 本邦基準判定 |
|---|---|
| なし | - |
| 軽微な紅斑 | ± |
| 紅斑 | + |
| 紅斑+浮腫 | ++ |
| 紅斑+浮腫+水疱、丘疹等 | +++ |
| 大水疱 | ++++ |
試験結果
- アウレオバシジウム M‐P04 の判定表
- 精製水の判定表
アウレオバシジウム M‐P04 の判定表
| 被験者 № | 年齢 | 性別 | 除去後1時間後 | 除去24時間後 |
|---|---|---|---|---|
| 1 | 55 | ♀ | - | - |
| 2 | 54 | ♀ | - | - |
| 3 | 53 | ♀ | - | - |
| 4 | 53 | ♂ | ± | - |
| 5 | 53 | ♀ | - | - |
| 6 | 46 | ♀ | - | - |
| 7 | 57 | ♂ | - | - |
| 8 | 54 | ♀ | - | - |
| 9 | 36 | ♂ | - | - |
| 10 | 55 | ♀ | - | - |
| 11 | 30 | ♂ | - | - |
| 12 | 42 | ♀ | - | - |
| 13 | 40 | ♂ | - | - |
| 14 | 46 | ♀ | - | - |
| 15 | 42 | ♀ | - | - |
| 16 | 37 | ♀ | - | - |
| 17 | 54 | ♂ | - | - |
| 18 | 55 | ♂ | - | - |
| 19 | 46 | ♂ | - | - |
| 20 | 43 | ♀ | - | - |
| 21 | 56 | ♀ | - | - |
| 22 | 46 | ♂ | - | - |
| 23 | 50 | ♀ | - | - |
| 24 | 45 | ♂ | - | - |
| 25 | 36 | ♀ | - | - |
| 26 | 55 | ♀ | - | - |
| 27 | 52 | ♀ | - | - |
| 28 | 44 | ♀ | - | - |
| 29 | 51 | ♀ | - | - |
| 30 | 41 | ♀ | - | ± |
| 31 | 44 | ♂ | - | - |
| 32 | 39 | ♂ | - | - |
| 33 | 43 | ♂ | - | - |
| 34 | 30 | ♂ | - | - |
| 35 | 51 | ♀ | - | - |
| 36 | 47 | ♀ | - | - |
| 37 | 37 | ♀ | - | - |
| 38 | 43 | ♀ | - | - |
| 39 | 28 | ♀ | - | - |
| 40 | 46 | ♀ | - | - |
精製水の判定表
| 被験者 № | 年齢 | 性別 | 除去後1時間後 | 除去24時間後 |
|---|---|---|---|---|
| 1 | 55 | ♀ | - | - |
| 2 | 54 | ♀ | - | - |
| 3 | 53 | ♀ | - | - |
| 4 | 53 | ♂ | ± | ± |
| 5 | 53 | ♀ | - | - |
| 6 | 46 | ♀ | - | - |
| 7 | 57 | ♂ | - | - |
| 8 | 54 | ♀ | - | - |
| 9 | 36 | ♂ | - | - |
| 10 | 55 | ♀ | - | - |
| 11 | 30 | ♂ | - | - |
| 12 | 42 | ♀ | - | - |
| 13 | 40 | ♂ | - | - |
| 14 | 46 | ♀ | - | - |
| 15 | 42 | ♀ | - | - |
| 16 | 37 | ♀ | - | - |
| 17 | 54 | ♂ | - | - |
| 18 | 55 | ♂ | - | - |
| 19 | 46 | ♂ | - | - |
| 20 | 43 | ♀ | - | - |
| 21 | 56 | ♀ | - | - |
| 22 | 46 | ♂ | - | - |
| 23 | 50 | ♀ | - | - |
| 24 | 45 | ♂ | - | - |
| 25 | 36 | ♀ | - | - |
| 26 | 55 | ♀ | - | - |
| 27 | 52 | ♀ | - | - |
| 28 | 44 | ♀ | - | - |
| 29 | 51 | ♀ | - | - |
| 30 | 41 | ♀ | ± | ± |
| 31 | 44 | ♂ | - | - |
| 32 | 39 | ♂ | - | - |
| 33 | 43 | ♂ | - | - |
| 34 | 30 | ♂ | - | - |
| 35 | 51 | ♀ | - | - |
| 36 | 47 | ♀ | - | - |
| 37 | 37 | ♀ | - | - |
| 38 | 43 | ♀ | - | - |
| 39 | 28 | ♀ | - | - |
| 40 | 46 | ♀ | - | - |
試料除去 1 時間後において、±反応をアウレオバシジウム M‐P04 に1名、精製水に2名認めた。試料除去24時間後において、±反応をアウレオバシジウム M‐P04 に1名、精製水に2名認めた。
結論
これまでの試験結果から、アウレオバシジウム M‐P04 は精製水に比較してパッチテストにおける皮膚刺激性は低く、しかも±反応を試料除去1時間後および 24 時間後にそれぞれ1名ずつ認めたのみで、+以上の反応は認められなかった。これまでの結果から、アウレオバシジウム M‐P04 の使用によって重篤な皮膚刺激を生じる可能性は低いと考えた。
安全性試験
研究課題「アウレオバシジウム M-P04」(黒酵母発酵グルカン)の化粧品利用における安全性試験
- 試験実施機関
- 株式会社バイオトクステック(Biotoxtech Co.,Ltd.) (韓国)
- GLP
- 本試験は‘OECD Principles of Good Laboratory Practice(as revised in 1997)’を遵守し実施した。
試験項目
1.細菌を用いる復帰突然変異試験
被験物質である「アウレオバシジウム M‐P04」の変異原性について、ネズミチフス菌株(TA98,TA100,TA1535,TA1537)および大腸菌菌株(WP2uvrA(pKM101))を用いて検討した。
被験物質の各試験菌株に対する生育阻害の有無および被試験物質の析出を確認するため、最高容量を5000 g/plate と設定し、以下公比 2 として計 5 用量の被験物質群、陰性および陽性対照群を用いて用量設定試験を実施した。
用量設定試験の結果、最高容量の 5000 g/plate を含む全用量において、代謝活性化の有無に関わらず、用いた全菌株で復帰変異コロニー数の減少、生育阻害などの試験菌株に対する毒性、および被験物質の析出が認められなかった。したがって、本試験の最高用量を全試験菌株について生育阻害および析出が認められなかった5000 g/plate と設定し、以下公比 2 として計 5 用量の被験物質群を設定した。また、陰性および陽性対照群を置いた。
本試験の結果、各試験菌株の被験物質群の復帰変異コロニー数は、代謝活性化の有無に関わらず用量依存性ならびに陰性対照群の 2 倍以上の増加は認められなかった。また、全試験菌株において用量設定試験との再現性が確認された。なお、最高用量の 5000 g/plate を含む全用量において代謝活性化の有無に関わらず、用いた全菌株で生育阻害および被験物質の析出は認められなかった。陰性対照群及び陽性対照群の復帰変異コロニー数の平均値が背景データの範囲に入っており、陽性対策群では当該用量で各菌株の特徴を確認できる増加が確認された。また、被験物質群において各菌株当り少なくとも 4 用量以上で復帰変異コロニー数が確認されたことから、試験が適切に実施されたと判断した。なお、用量設定試験および本試験で実施した無菌試験では、雑菌の汚染は認められなかった。
以上の結果より、当該試験条件下において「アウレオバシジウム M‐P04」の変異原性は陰性であると判定した。
2.ウサギにおける眼粘膜刺激性試験
被験物質である「アウレオバシジウム M‐P04」の眼に対する刺激性を 15~16 週齢 NZW 種雄性ウサギを用いて検討した。
その結果、投与後 1、24、48 および 72 時間目の観察において、角膜、虹彩および結膜に眼刺激性の変化は認められなかった。被験物質の MMTS は 0 であり、Kay and Calandra の眼に対する刺激性の暫定的評価に従い‘刺激性なし’と分類された。投与後 24 時間目の MTS は 0 であることから、最終評価も同様に、‘刺激性なし’と分類された。観察時期を通じて、一般状態の変化、死亡例および体重において、全例で被験物質投与による影響は認められなかった。
以上の結果より、本試験条件下において「アウレオバシジウム M‐P04」はウサギの眼に対して刺激性
は無いものと結論した。
3.ウサギにおける2週間連続皮膚刺激性試験
被験物質である「アウレオバシジウム M‐P04」の連続皮膚刺激性を 15~17 週齢 NZW 種雄性ウサギを用いて検討した。
その結果、被験物質の投与部位には、いずれの観察時点においても紅斑および浮腫等の皮膚刺激性の変化は認められなかった。観察期間を通じて一般状態の変化、死亡例および体重において、全例で被験物質投与による影響は認められなかった。
以上の結果より、本試験条件下において「アウレオバシジウム M‐P04」の連続皮膚刺激性はないものと結論した。
4.ウサギにおける皮膚一次刺激性試験
被験物質である「アウレオバシジウム M‐P04」の皮膚一次刺激性を 16~17 週齢 NZW 種雄性ウサギを用いて検討した。
その結果、被験物質の健常皮膚と擦過皮膚の投与部位には、いずれの観察時間にも皮膚刺激性の変化は全く認められなかった。観察時間の皮膚一次刺激指数(P.I.I.)は’0’であったことから、Draize の皮膚反応の測定基準に従うと、「アウレオバシジウム M‐P04」は‘無刺激物(Non irritant)’と分類された。
以上の結果より、本試験条件下において、「アウレオバシジウム M‐P04」の皮膚一次刺激性はないものと結論した。
5.ラットにおける単回経口投与毒性試験(限度試験)
被験物質である「アウレオバシジウムM‐P04」の2000 mg / 10 ml/kgを6週齢Sprague-Dawley(Crl:CD(SD))系雌雄ラットに単回強制経口投与し、毒性徴候および概略の致死量について検討した。
対照群には注射用水を 10ml/kg 投与した。死亡推移および一般状態では、対象群および被験物質投与群の雌雄には観察期間を通じて死亡例はなく、一般状態の変化も認められなかった。
体重では、対照群および被験物質投与群の雌雄全例に順調な増加が認められた。剖検では、対照群および被験物質投与群の雌雄全例の体表、頭蓋腔内、胸腔内および腹腔内の諸器官に肉眼的異常は認められなかった。
以上の結果より、「アウレオバシジウム M‐P04」のラットにおける単回経口投与毒性試験で、被験物質による毒性徴候は観察されず、概略の致死量は雌雄ともに 2000 mg / kg 以上であると結論した。
6.モルモットにおける皮膚感作性試験
被験物質である「アウレオバシジウム M‐P04」の皮膚感作性を Hartley 系雄性モルモットを用いてMaximization 法により検討した。
群構成は、被験物質感作群(10 匹)、被験物質悲感作群(5 匹)、陽性物質感作群(5 匹)および陽性物質非感作群(5 匹)の計4群とした。なお、本被験物質の予備試験の経皮投与において皮膚反応が認められなかったので、陽性物質感作群を除いた各群に再感作 24 時間前に起炎剤塗布を行った。被験物質感作群では、10 例全例で皮膚反応は認められなかった。被験物質悲感作群では、5 例全例で皮膚反応は認められなかった。陽性物質感作群では、5 例全例で皮膚反応は認められなかった。観察期間を通して死亡例はなく、一般状態の変化および体重において、各群全例で被験物質投与による影響は認められなかった。
以上の結果より、アウレオバシジウム M‐P04 の皮膚感作性は陰性であると結論した。
7.ほ乳類培養細胞を用いる染色体異常試験
被験物質である「アウレオバシジウム M‐P04」について、チャイニーズ・ハムスター線維芽細胞株(CHL/IU 細胞)を用いて染色体誘発性を検討した。
被験物質を注射用水に溶解し、0(陰性対照群)および 5、10、50、100、250、500、1000、2500、5000μg/ml の用量について、短時間処理(代謝活性化非存在下、存在下)並びに連続処理法で細胞増殖抑制試験を行った。その結果、いずれも細胞毒性を示さなかったことから、染色体異常試験では、3 処理系列とも、5000μg/ml を最高用量とし、以下公比 2 で、2500 および 1250μg/ml の被験物質群を設定した。また、陰性対照群および陽性対照群を設けた。
顕微鏡観察の結果、各処理系列における被験物質のいずれの用量も、染色体異常を持つ細胞の出現頻度は 5%未満であり、陰性対照群と比較して有意な増加は認められなかった。また、処理終了時に被験物質の析出は認められなかった。各処理系列の陽性対照群では、染色体異常を持つ細胞の出現頻度は10%以上であり、陰性対照群と比較して有意な増加が認められたことより、本試験は適切に実施されたと判断した。
以上の結果より、当該試験条件下において、被験物質であるアウレオバシジウム M‐P04 はほ乳類培養細胞において染色体構造異常および数的異常を誘発しないと結論した。
紫外線障害防止および抗炎症効果について
研究課題アウレオバシジウム M-P04 の化粧品利用における有効性試験
- 共同研究者
- 長谷川武夫(鈴鹿医療科学大学・大学院、保健衛生学研究科)
研究内容
「アウレオバシジウム M-P04」の持つ紫外線による細胞損傷防止効果、抗炎症効果について ICR マウスを用いて実験を行った。
6 週齢、雄 ICR マウスの背中皮膚に紫外線を照射し、紫外線照射単独群、「アウレオバシジウム M-P04」塗布+紫外線照射併用群、市販日焼け防止剤+紫外線照射併用群の 3 群について皮膚炎症を組織学的検査によって検討した。
結果
皮膚を形成する組織(表面から表皮、真皮、皮下組織で形成されている)の内で表層の表皮層と真皮層に「アウレオバシジウム M‐P04」は紫外線防護効果を示した。
「アウレオバシジウム M‐P04」は表皮組織の淡明層、顆粒層を主に防護し、角質化(しわ)を予防している。
| 皮膚組織 | 紫外線単独群 | 紫外線+アウレオバシジウム M-P04 |
|---|---|---|
| 表皮層 | 強度角質層剥離 | 軽度角質層剥離 |
| 真皮層 | 血管拡張、血管損傷 | 血管拡張 |
| 皮下組織 | コラーゲン微弱減少 | コラーゲン正常 |
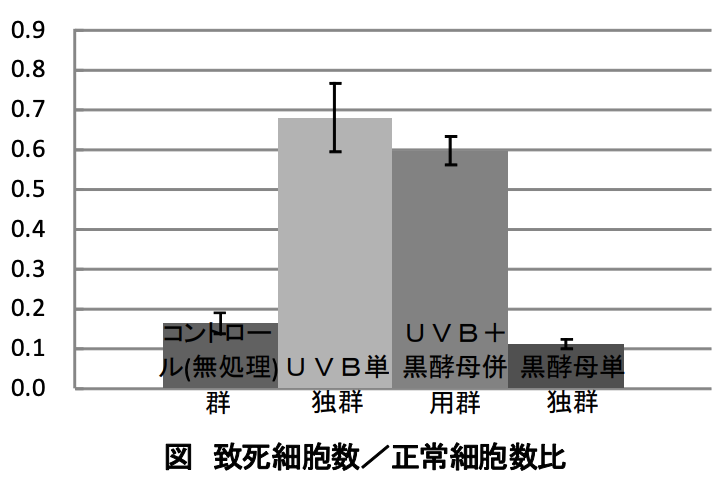
グラフは、致死細胞数/正常細胞数の比を示す。
縦軸は死亡細胞数の割合を示し、高いグラフ程細胞死が多く発生している事を示し、低い程、障害が少ない事(紫外線の影響が少ない)を示す。
この事から、無処理コントロール群より黒酵母添加群は細胞死が低下し、細胞に対して黒酵母は防護の作用があると言える。
一般的には無処理コントロール群は細胞死が無くグラフは一番低い状態に成るが、今回は腫瘍細胞であるメラノーマ細胞を用いたため、幾分かの細胞死が見られる。紫外線を当てると 68%まで死亡率が増加するが、黒酵母を培地に添加する事で死亡率は59%に低下し、黒酵母による紫外線障害の予防が観測されている。
今回は紫外線を最高強度で照射し、真夏の太陽光線以上に強い紫外線を照射したため、防護作用が低下したと思われる。日常の太陽光程度の紫外線量で実験すれば、防護効果は更に現われると思われる。